O-糖基化作为常见的翻译后修饰,参与着各种重要的生命活动。与N-糖修饰相比,O-糖具有丰度低、核心结构复杂且多样等特点,由于缺乏恒定修饰序列(可随机修饰在丝氨酸、苏氨酸和羟赖氨酸上)以及缺乏特异性切O-糖工具酶,蛋白O-糖的鉴定一直被视为行业难题。
CD24(Cluster of Differentiation 24)是一种高度糖基化的糖基磷脂酰肌醇锚定表面蛋白,高表达于多种恶性肿瘤表面,利用其高度糖基化的结构与肿瘤相关巨噬细胞上的抑制性受体Siglec-10(唾液酸结合免疫球蛋白型凝集素)相互作用,发出“don't eat me”信号,促进免疫逃逸。
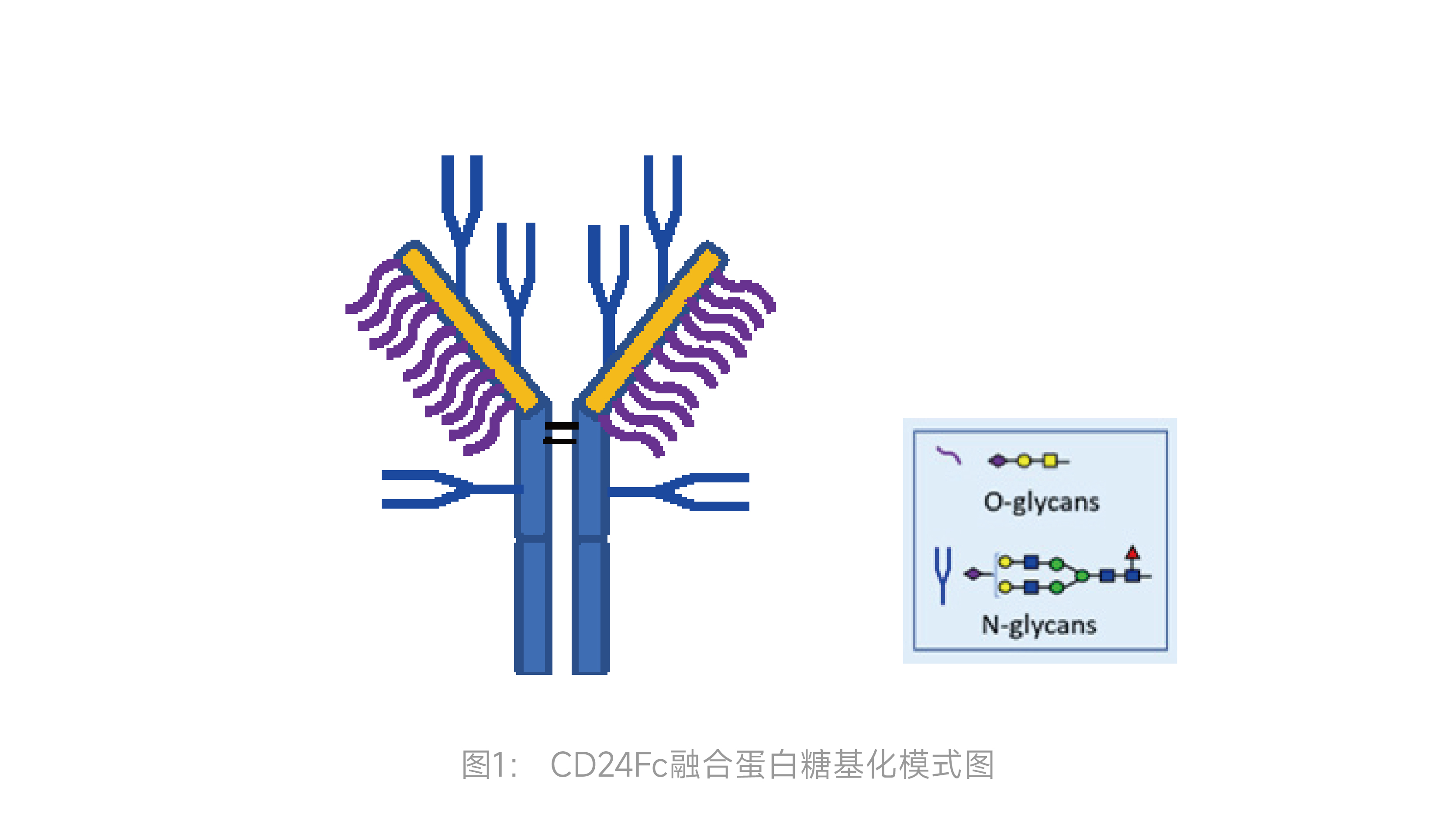
CD24Fc是一种重组人CD24胞外域和人免疫球蛋白IgG1 Fc端的融合蛋白。既可以阻断CD24与Siglec-10相互作用,来增强巨噬细胞对表达CD24的肿瘤细胞吞噬作用,又可以增强体内半衰期,同时Fc融合蛋白形式的二聚体也增强了药物稳定性。但由于CD24存在高度密集的N-/O-糖基化修饰位点,复杂的糖型(图1),使得CD24Fc药物研发中糖分析异乎寻常地困难。
近日,汉腾生物欧洲子公司FyoniBio的Robert Wilmanowski博士等人的研究成果《Precise O‑Glycosylation Site Localization of CD24Fc by LC-MS Workflows》刊登在Analytical Chemistry杂志,首次利用多种酶切策略结合LC-MS的CID裂解和EThcD裂解技术互补分析,在糖肽层面,精确定位了CD24Fc蛋白中所有O-糖修饰位点和糖型分布,对CD24Fc融合蛋白的药物开发有着重要意义,同时也为致力于O-糖组成,O-糖位点分析的研究者们提供了新的方法。
二、分析流程
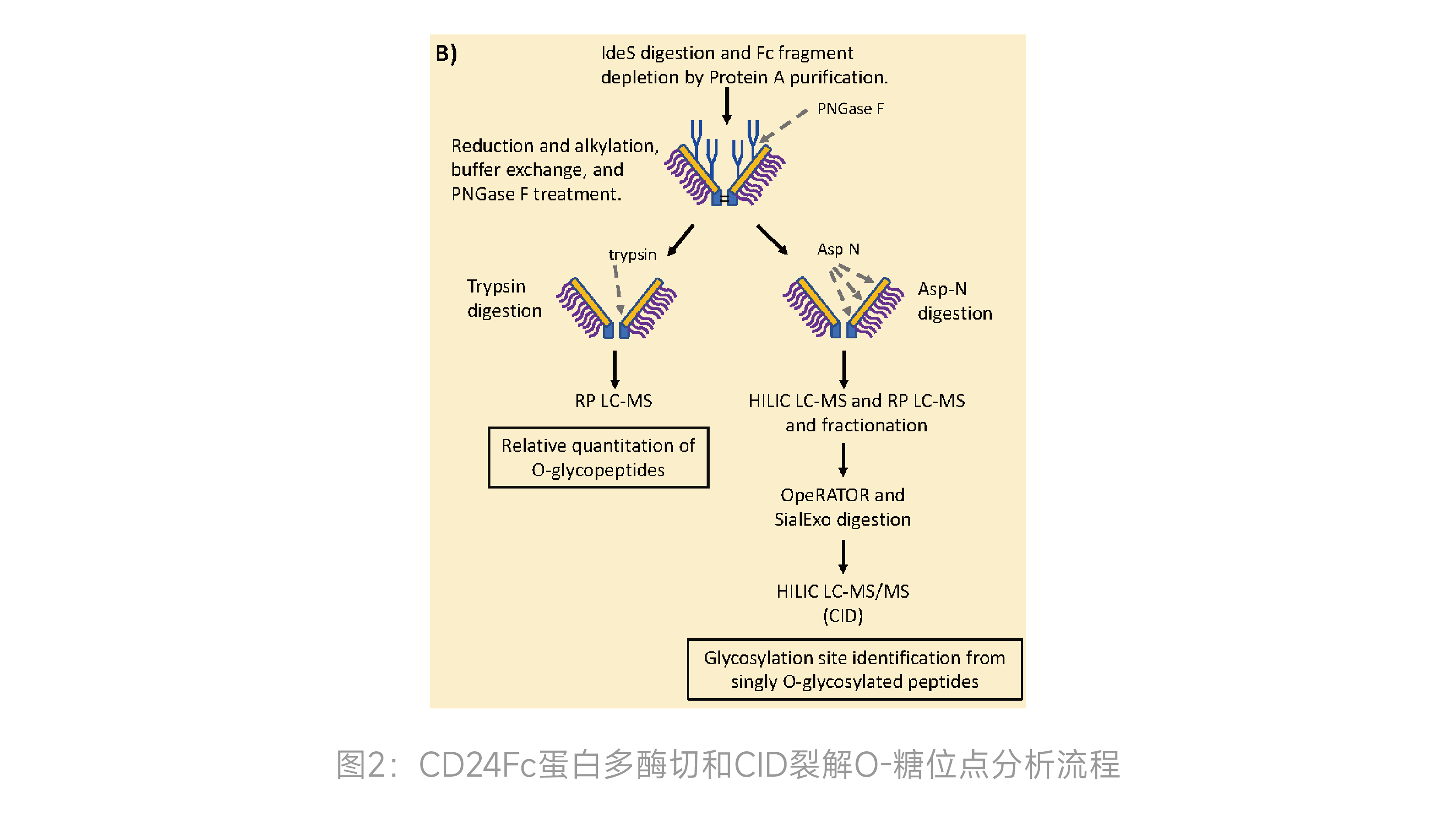
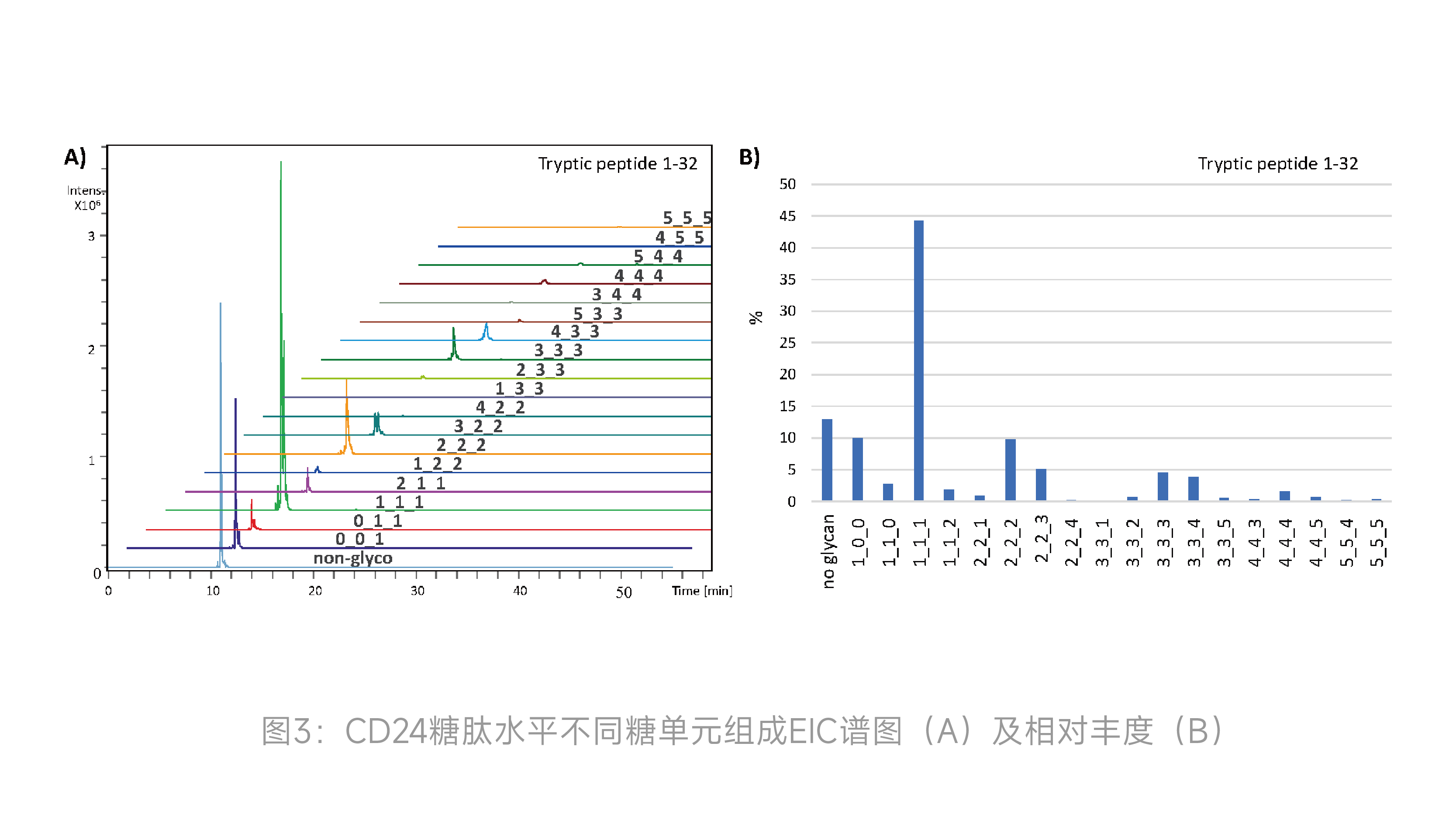
为降低目标蛋白复杂度,研究者采用IdeS酶切结合ProA纯化,在亚基层面富集到CD24蛋白后采用PNGaseF和Trypsin酶切。如图2(左)所示,得到去除N-糖含完整CD24序列的结构域组分,利用LC-MS技术,针对包含1-32位氨基酸的糖肽片段进行分析,获得CD24(CD24部分仅含31个氨基酸)上所有O-糖单元组成及相对含量。(见图3,x_y_z分别代表NeuAc(x)_Hex(y)_HexNAc(z) 糖单元的个数)。
由于OpeRATOR酶具备特异性酶切O-糖基化后的S/T的N端肽键的特性(联合SialEXO唾液酸切除酶可提高效率)。首先使用Asp-N将CD24序列切成3段,然后利用SialEXO和OpeRATOR酶切特性,继续缩短糖肽长度,且再次酶切所得的肽段N端氨基酸即为O-糖基化位点。如图2(右)所示,实验结果表明,CD24主要O-糖位点为T25和T15,而T4,T5,T7,S12,S28存在少量的O糖修饰。

此外,研究者还采用OpeRATOR/SialEXO酶结合PNGaseF和Lys-C酶切,获得含不同氨基酸的糖肽,结合LC-MS/MS(EThcD模式)对O-糖位点精细研究鉴定,可得T25,T15为主要O-糖修饰位点,T4, T5,S12,S14,S16,S18,T28存在少量O糖修饰,而T3,T7,T11存在微量的O-糖修饰。
三、鉴定结果
综合两种分析流程(LC-MS CID和EThcD裂解技术),结合多种酶(IdeS, Asp-N, PNGaseF, OpeRATOR, SialEXO, Trypsin, Lys-C),确定了CD24Fc融合蛋白的O-糖基化位点和O-糖基化相对修饰程度,如图5所示,结果显示CD24Fc蛋白共包含12个O-糖基化位点,其中 7个O-糖基化位点在两种分析流程均得到验证,另有5个O-糖基化位点可以被ETHcD裂解分析流程验证,如图5(下)。
该研究首次精确确证了CD24 O-糖基化位点和相对修饰程度,填补了CD24蛋白O-糖基化修饰的空白领域,拓宽了LC-MS在糖肽水平O-糖基化研究策略,同时也为CD24信号疗法的药物研发提供坚实可靠的理论结构依据。

关于FyoniBio GmbH
FyoniBio GmbH是汉腾生物全资欧洲子公司,专注于生物大分子药物开发及分析服务 ,核心团队成员具备20年以上的生物制药开发经验。公司可为全球生物制药客户提供细胞系开发、上下游工艺开发、分析方法开发及临床生物检测等专业服务。目前已为多家跨国药企及生物技术公司提供高品质的生物药开发及分析服务。
网址:www.fyonibio.com
汉腾生物拥有全流程全方位的生物药大分子分析检测平台,完善的质量保证体系,完全依从相关法规,保证操作合规性及数据的完整性,可支持产品表征研究、了解分子的关键质量属性,制定可靠的质量控制策略等。我们时刻关注最新的法规政策,不断升级技术配备,以便更快、更好、更全地为客户提供一站式的分析解决方案。涵盖单抗、双抗、重组/融合蛋白、蛋白疫苗、mRNA疫苗、AAV 载体、质粒、重组/合成多肽、核酸药物、ADCs等分析研究。

参考文献:Precise O‑Glycosylation Site Localization of CD24Fc by LC-MS Workflows
文献链接:https://www.nstl.gov.cn/paper_detail.html?id=0258b1488e32fa235e35cca357eeec60


